Nat Commun:靶向大脑中的小胶质细胞有望恢复与阿尔茨海默病相关的脂质失衡
来源:生物谷原创 2025-11-27 15:46
这项研究表明,阿尔茨海默病不仅仅是关于淀粉样斑块和tau蛋白缠结。它还涉及脂质平衡的破坏,其中小胶质细胞、星形胶质细胞和神经元各自扮演着不同的角色。
一个多世纪前,Alois Alzheimer注意到大脑脂肪出现了异常变化,他将其描述为"脂质颗粒(lipoid granules)",同时伴有β-淀粉样蛋白斑块的积聚和tau蛋白缠结。这些观察结果最终导致了阿尔茨海默病及相关痴呆症的确认。自那时起,大多数阿尔茨海默病研究都聚焦于淀粉样蛋白和tau蛋白,而大脑脂质异常则很少受到关注。

由圣安东尼奥德克萨斯大学健康科学中心与加州大学欧文分校合作进行的一项新研究表明,大脑脂肪(即脂质)的变化在阿尔茨海默病的发生和进展中起着重要作用。脂质失衡会影响淀粉样蛋白的积聚方式,而某些调控脂质代谢的基因也与阿尔茨海默病的风险相关。
"大脑是一个独特的器官,"该研究的共同负责人、圣安东尼奥德克萨斯大学朗医学院细胞与整合生理学系助理教授Juan Pablo Palavicini博士说。"与大多数其他富含蛋白质的器官不同,大脑干重的一半以上由不同种类的脂质构成,包括胆固醇、磷脂和鞘脂。在阿尔茨海默病中,我们观察到这些脂质遭受了严重破坏,然而大多数研究却只关注基因和蛋白质。"
这项发表在《自然·通讯》上的研究揭示了大脑免疫细胞——小胶质细胞——如何控制其中部分脂质变化。根据操作方式的不同,小胶质细胞既可以帮助维持平衡,也可能加重疾病。
测试小胶质细胞的作用
科学家们使用阿尔茨海默病小鼠模型测试了两种清除小胶质细胞的方法。一种是用一种药物处理小鼠,几乎消除了所有小胶质细胞;另一种是使用经过基因改造、缺乏小胶质细胞的小鼠。这些策略使研究人员能够将小胶质细胞引起的影响与其他脑细胞引起的影响区分开来。
"我们想了解是哪些细胞驱动了这些脂质变化,"Palavicini说。"有些脂质水平上升,有些下降,但哪些细胞类型该对此负责?通过移除小胶质细胞,我们就能看出哪些变化依赖于它们,哪些不依赖。"
研究团队将小鼠研究的结果与来自患有和未患阿尔茨海默病的人类尸检脑样本进行了比较。他们发现,淀粉样蛋白的积聚 dramatically 改变了大脑的脂质模式。有两类脂质尤为突出:与炎症和氧化应激相关的溶血磷脂(LPC和LPE),以及帮助调控细胞"回收中心"(即溶酶体)的脂质——双(单酰基甘油)磷酸酯(BMP)。
研究团队发现,一种含有花生四烯酸的BMP(AA-BMP)在淀粉样斑块附近积聚,而长期移除小胶质细胞阻止了AA-BMP的积聚,这表明小胶质细胞驱动了这些变化。
"BMP,尤其是在大脑中的BMP,至今仍未得到充分理解,"Palavicini说。"它在溶酶体中形成亚结构,吸引蛋白质来分解受损的脂质。没有小胶质细胞,AA-BMP水平会下降,这可能会干扰大脑的清理过程。"
颗粒蛋白前体的关键作用
由小胶质细胞和神经元共同产生的颗粒蛋白前体在该研究中显现为关键的脂质调节因子。在阿尔茨海默病条件下,颗粒蛋白前体水平升高,并且与AA-BMP的积聚密切相关。移除小胶质细胞降低了斑块附近的颗粒蛋白前体和AA-BMP水平,这表明小胶质细胞来源的颗粒蛋白前体有助于调节脂质平衡。
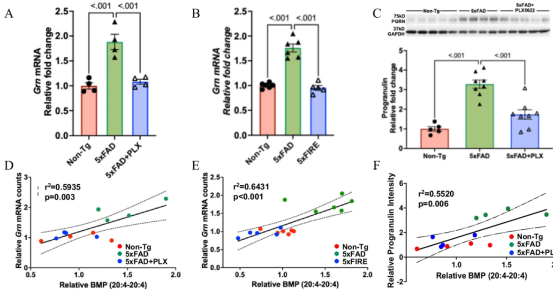
"在阿尔茨海默病大脑中,重要的可能不是降低BMP,而是维持或支持其水平,"Palavicini说。"颗粒蛋白前体有助于维持这种脂质并保护神经元。提升颗粒蛋白前体的疗法有可能恢复平衡,支持大脑健康。"
其他脑细胞的影响
并非所有脂质都受小胶质细胞控制。LPC和LPE的水平主要受星形胶质细胞和神经元的影响。LPC的积聚与星形胶质细胞的活化和酶活性有关,而LPE的增加则与氧化应激和抗氧化防御能力减弱有关。
"尽管我们曾假设小胶质细胞驱动了这些炎症性脂质的积聚,但实际上是其他细胞类型,包括星形胶质细胞,在起作用,"Palavicini说。"这种区分有助于我们理解治疗应靶向哪些细胞,并揭示了阿尔茨海默病中脂质调控的复杂性。"
小胶质细胞保护髓鞘和神经元
该研究还揭示,小胶质细胞也有助于维持髓鞘(神经元周围的保护性涂层)的稳定。在淀粉样蛋白应激下,通过基因方法移除小胶质细胞会减少与髓鞘相关的脂质。
"小胶质细胞在帮助神经元,如果移除它们,神经元似乎会经历更多的氧化应激,"Palavicini说。"这就是为什么当小胶质细胞缺失时,某些脂质水平会升高。在大多数情况下,移除小胶质细胞是有害的,这有点出乎意料,但也揭示了它们对大脑脂质代谢是何等重要。"
更完整的阿尔茨海默病图景
这项研究表明,阿尔茨海默病不仅仅是关于淀粉样斑块和tau蛋白缠结。它还涉及脂质平衡的破坏,其中小胶质细胞、星形胶质细胞和神经元各自扮演着不同的角色。小胶质细胞维持像BMP这样的保护性脂质并支持髓鞘,而星形胶质细胞和神经元则驱动其他变化,包括溶血磷脂的积聚和氧化应激。
"了解哪些细胞调控哪些脂质,为开发更精准的疗法打开了大门,"Palavicini说。"通过将脂质平衡与淀粉样蛋白和tau蛋白一同作为靶点,我们可以制定出更好的策略来保护神经元,并有可能减缓或预防阿尔茨海默病。"(生物谷Bioon.com)
参考文献:
Ziying Xu et al, Microglia-specific regulation of lipid metabolism in Alzheimer's disease revealed by microglial depletion in 5xFAD Mice, Nature Communications (2025). DOI: 10.1038/s41467-025-64161-z.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


